Агрегатное состояние
Агрегатные состояния вещества — состояния одного и того же вещества, отличающихся характером теплового движения частиц (атомов или молекул). Обычно различают три агрегатных состояний вещества: газ, жидкость и твердое тело. Иногда к агрегатным состояниям относят и плазменное состояние. Вещество в любом агрегатном состоянии существует при определенных внешних условиях (температура, давление), изменение которых приводит к скачкообразному переходу из одного агрегатного состояния в другое. Также изменение состояния вещества называется фазовым переходом[1].
Газообразное состояние
Газообразное агрегатное состояние вещества характеризуется тем, что вещество находится в состоянии газа. Молекулы вещества находятся довольно свободно и перемещаются друг относительно друга с высокой скоростью. В газообразном состоянии вещество не имеет формы или объема, оно заполняет пространство, в котором находится. Примерами газообразных веществ являются кислород, азот, водород и другие.
Жидкое состояние
При изменении условий: повышенное давление или снижение температуры, газы могут превратиться в жидкость, претерпевая изменения в своей структуре и поведении. Жидкость, обладает определенным объемом, но при этом обычно принимает форму сосуда, в котором она находится. Молекулы жидкости находятся в постоянном, хоть и свободном взаимодействии друг с другом, что позволяет им свободно перемещаться. Если капля попадет на поверхность, она со временем испарится, изменяя свою структуру. Это напоминает нам о законе сохранения массы и энергии, подчеркивая непрерывный цикл изменений состояний вещества. Свойства жидкостей: текучесть и вязкость. В отсутствие гравитации, жидкость примет форму шара, под воздействием поверхностного натяжения. Большинство из них подчиняются установленному Ньютоном закону вязкости, который был открыт в XIX веке[2].
Твердое состояние
Твердое состояние является основным агрегатным состоянием вещества, частицы материи находятся близко друг к другу и имеют фиксированное положение в кристаллической решетке. Твердые вещества обычно имеют определенную форму и объем, а их атомы или молекулы обладают минимальной подвижностью. Это состояние имеет огромное значение в науке и технике, так как многие материалы, используемые в повседневной жизни, являются твердыми. В твердом состоянии вещества возможны различные виды кристаллических и аморфных структур, каждая из которых обладает уникальными свойствами и характеристиками[1].
Плазма
Является четвёртым основным агрегатным состоянием вещества.
Плазма — ионизированный газ, в котором объемные плотности положительных и отрицательных электрических зарядов практически одинаковы, а концентрация заряженных частиц сравнительно велика. Образуется при электрическом заряде в газах, при нагревании газа до температуры, достаточной для термической ионизации. Обладает свойствами проводить электрический ток, отклоняться под воздействием магнитного поля и испускать свет. В состоянии плазмы находится подавляющая часть вещества Вселенной: звёзды, галактические туманности и межзвездная среда. Плазма называется «холодной», или низкотемпературной, и «горячей», или высокотемпературной, если температура её ионной компоненты равна 103 — 104 К и 106 — 107 К соответственно. Особый интерес представляет сверхвысокотемпературная плазма в связи с проблемой управляемых термоядерных реакций[2].
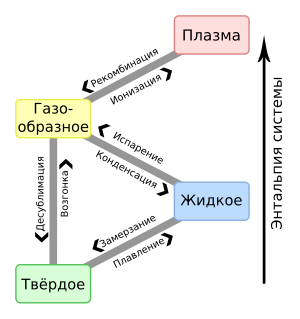
Фазовые переходы
Соприкасающиеся фазы могут превращаться (переходить) друг в друга. Переход вещества из одной фазы в другую называется фазовым переходом или фазовым превращением.
Существуют следующие фазовые переходы:
1) жидкость — пар;
2) жидкость — твердое тело;
3) твердое тело — пар.
Конденсация — процесс перехода вещества из газового состояния в жидкое состояние. Во время конденсации газ охлаждается до температуры, при которой молекулы теряют достаточно энергии для поддержания газового состояния и начинают сближаться, образуя жидкость. Этот процесс обратен испарению, при котором жидкость превращается в газ. Конденсация имеет множество практических применений, например, при кондиционировании воздуха, образовании облаков и дождя, производстве различных продуктов и технологии охлаждения.
Испарение — переход вещества из жидкого или твердого состояния в газообразное. Если нет внешних воздействий, испарение жидкостей происходит крайне медленно. Молекулы покидают жидкость из-за явления диффузии[3].
Плавление — процесс, при котором вещество переходит из твердого состояния в жидкое при достижении определенной температуры, называемой температурой плавления. При достижении этой температуры молекулы или атомы вещества начинают двигаться быстрее, таким образом переходя из упорядоченной кристаллической решетки твердого состояния в более хаотичное состояние жидкости. Температура плавления зависит от химического состава вещества и давления.
Кристаллизация — процесс, при котором от избыточного растворителя выпадают кристаллы растворенного вещества. В результате процесса кристаллизации происходит образование кристаллов из раствора или расплавленного состояния вещества. Этот процесс широко используется в химической и фармацевтической промышленности для получения чистых веществ или сорбции веществ из растворов.
Сублимация — процесс, при котором вещество прямо переходит из твердого состояния в газообразное состояние без прохождения через жидкое состояние. В процессе сублимации молекулы вещества нагреваются настолько, что они переходят из упакованного твердого состояния прямо в свободное газообразное состояние. Примерами сублимации могут служить сублимация сухофруктов, сублимация сульфата меди и так далее.
Десублимация — процесс, при котором вещество переходит из газообразного состояния в твердое состояние, минуя жидкую фазу. Процесс происходит при охлаждении газообразного вещества до температуры, при которой оно конденсируется прямо в твердую фазу без образования жидкости. Примером десублимации является переход паров наледи в снег в условиях низких температур[4].
Примечания
- ↑ 1,0 1,1 Александр Иванович Болсун. Краткий словарь физических терминов. — "Вышэйшая школа", 1979. — С. 17—259. — 416 с.
- ↑ 2,0 2,1 Болсун А. И., Рапанович Е. Н. Словарь физический и астрономических терминов: Для учащихся среднего и старшего школьного возраста. — "Народная асвета", 1986. — С. 11—113. — 232 с.
- ↑ Испарение. skysmart.ru. Дата обращения: 4 июня 2024.
- ↑ Брюханов А.В.,Пустовалов Г.Е.,Рыдник В.И. Толковый физический словарь.Основные термины. — "Русский язык", 1987. — С. 66. — 118 с.
Данная статья имеет статус «проверенной». Это говорит о том, что статья была проверена экспертом |